Аргентум, или серебро — металл и химический элемент, которому присвоен атомный номер 47 в периодической таблице Менделеева. Химическая формула металла — Ag. Серебро было исследовано человечеством еще в четвертом тысячелетии до нашей эры. Открытие этого металла обошлось без помощи ученых, поскольку он был найден человеком как самородное серебро. Причем самородки достигали весьма впечатлительных размеров. К примеру, в пятнадцатом столетии был добыт самородок массой свыше 20 тонн.
Однако добыча серебра требовала больше усилий по сравнению с теми, которые приходилось прикладывать для добычи золота. По этой причине на протяжении нескольких столетий серебро стоило дороже золота. Запасы серебряной руды на Земле на сегодня составляют свыше 550 тонн, причем государствами-лидерами в добыче серебра считаются:
- Перу.
- Австралия.
- Чили.
- Мексика.
Драгоценный металл содержится в коре Земли в концентрации 70 миллиграммов на тонну. В условиях природы аргентум встречается в большинстве случаев в рудных залежах в комбинации с другими элементами. В природе находится свыше пятидесяти видов серебряных руд, однако эффективными, с точки зрения экономики, считаются такие:
- самородное серебро;
- кюстелит;
- электрум;
- бромаргерит;
- прустит;
- агвиларит и другие.
Серебро может встречаться в природе совместно с золотом, и такое образование называется электрумом. Благородный металл в большом количестве сосредоточен в рудах, содержащих уран, висмут и никель.
Кристаллы серебра
Самородное серебро есть в сульфидных рудах, в которых оно образует мельчайшие кристаллы, распыленные среди других металлов, из которых состоят руды. На изломах кристаллы имеют неровную угловатую поверхность, что делает их похожими на крючки. Это находка, которая встречается в природных условиях гораздо реже золота. Причем внешний вид таких самородков весьма необычный. Из-за своей пластичности серебро образует самородки, напоминающие решетки, трубочки, ветви и жгуты. По этой причине такое серебро не используется в промышленных целях, а служит лишь экспонатом в музеях.
Серебро, свойства атома, химические и физические свойства.
Ag 47 Серебро
107,8682(2) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s1
Серебро — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 47. Расположен в 11-й группе (по старой классификации — побочной подгруппе первой группы), пятом периоде периодической системы.
Атом и молекула серебра. Формула серебра. Строение атома серебра
Цена на серебро
Изотопы и модификации серебра
Свойства серебра (таблица): температура, плотность, давление и пр.
Физические свойства серебра
Химические свойства серебра. Взаимодействие серебра. Химические реакции с серебром
Получение серебра
Применение серебра
Таблица химических элементов Д.И. Менделеева
Исторические факты о серебре
Существует легенда, что первые серебряные рудники были открыты в 968 г. никем иным как основателем Священной Римской империи восточно-франкским королём Оттоном I Великим. Легенда гласит, что однажды король послал своего егеря в лес на охоту. Во время охоты тот привязал коня к дереву, который в ожидании хозяина разрыл копытами землю, где оказались необычные светлые камни. Император понял, что это серебро и повелел основать на этом месте рудник. Существуют данные, что этот богатейший рудник разрабатывался еще спустя шесть веков. Об этом свидетельствуют записи немецкого врача и металлурга Георга Агриколы (1494–1555). Вообще Центральная Европа была очень богата залежами серебряных самородков. В Саксонии в 1477 году был найден один из самых больших самородков в истории массой до 20 тонн! Из серебра добытого в Чехии, близ города Иоахимсталя, были отчеканены миллионы европейских монет. Поэтому их так и называли — «иоахимсталер»; со временем слово укоротилось до «талера». В России это название переиначили на свой лад и у нас они назывались «ефи́мками». Серебряные талеры были самой распространенной европейской монетой в истории, от этого название пошло современное название «доллар».
Чешский богемский Иоахимсталер
Европейские серебряные рудники были настолько богаты, что расход серебра измерялся в тоннах! Но т.к. основная масса европейских серебряных рудников была открыта в XIV-XVI вв., то к настоящему времени они уже истощены. После открытия Америки оказалось, что этот континент очень богат на серебро. Его залежи были обнаружены в Чили, Перу и Мексике. Аргентина даже получила название по латинскому имени серебра. Тут нужно указать на очень интересный факт. Географические названия химических элементов обычно давались элементу от названия какого-то места, например, гафний назван так от латинского наименования города Копенгаген, в котором он был открыт, географические названия имеют элементы полоний, рутений, галлий и другие. Тут же произошло все с точностью наоборот. Страна была названа по имени химического элемента! Это единственный подобный случай в истории. Самородки серебра находят в Америке и в настоящее время. Один из них был открыт уже в XX веке в Канаде. Этот самородок был длиной 30 метров и глубиной 18 метров! После освоения этого самородка оказалось, что он содержал 20 тонн чистого серебра!
Атом и молекула серебра. Формула серебра. Строение атома серебра:
Серебро (лат. Argentum) – химический элемент периодической системы химических элементов Д. И. Менделеева с обозначением Ag и атомным номером 47. Расположен в 11-й группе (по старой классификации – побочной подгруппе первой группы), пятом периоде периодической системы.
Серебро – металл. Относится к группе переходных металлов, а также к драгоценным металлам и металлам платиновой группы.
Серебро обозначается символом Ag.
Как простое вещество серебро при нормальных условиях представляет собой ковкий, пластичный металл серебристо-белого цвета.
Молекула серебра одноатомна.
Химическая формула серебра Ag.
Электронная конфигурация атома серебра 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s1. Потенциал ионизации (первый электрон) атома серебра равен 731 кДж/моль (7,576234(25) эВ).
Строение атома серебра. Атом серебра состоит из положительно заряженного ядра (+47), вокруг которого по пяти оболочкам движутся 47 электронов. При этом 46 электронов находятся на внутреннем уровне, а 1 электрон – на внешнем. Поскольку серебро расположен в пятом периоде, оболочек всего пять. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внутренняя оболочка представлены s- и р-орбиталями. Третья и четвертая – внутренние оболочки представлены s-, р- и d-орбиталями. Пятая – внешняя оболочка представлена s-орбиталью. На внешнем энергетическом уровне атома серебра на s-орбитали находится один неспаренный электрон. В свою очередь ядро атома серебра состоит из 47 протонов и 61 нейтрона. Серебро относится к элементам d-семейства.
Радиус атома серебра (вычисленный) составляет 165 пм.
Атомная масса атома серебра составляет 107,8682(2) а. е. м.
Серебро, будучи благородным металлом, отличается относительно низкой реакционной способностью.
Сера, свойства атома, химические и физические свойства
Серебро в природе
Серебро является достаточно редким элементом, в литосфере его содержится всего около 0,000001%. Это примерно в тысячу раз меньше, чем содержание меди в земной коре. Несмотря на редкость, серебро чаще встречается в виде самородков, поэтому то оно и было известно с незапамятных времен. Сейчас самородное серебро стало редкостью, основная часть серебра находится в разнообразных минералах, основным из которых является аргентит Ag2S. Также большая часть находится в так называемых полиметаллических рудах, в них серебро соседствует с такими металлами как свинец, цинк и медь.
Историческая справка
Люди знакомы с серебром с древнейших времен, так как оно было популярным самородком и не требовало плавления руды. К древнейшим центрам добычи и обработки металла относят доисторическую Сардинию, где он стал известен еще в период раннего энеолита.
Серебро включают археологические находки на разных континентах. На территории Древнего Египта нашли аксессуары, датированные 5,5–7 тысячелетиями. Металл тогда получали из древнейших месторождений в Сирии.
Элементу издревле присваиваются магические и целебные свойства. Из-за этого его ассоциировали с Луной, использовали алхимики.
По значимости среди драгоценных металлов серебро уступает только золоту. Очищать его люди научились примерно 2,5 тысячелетия назад. Раньше использовали большие ступы для измельчения руды — получали порошок, в котором серебро отделяли от разных примесей.
Стоимость драгоценного металла начала быстро расти после чеканки первых монет. Произошло это в Месопотамии еще за полтысячелетия до нашей эры. Серебром рассчитывались и на Руси — сначала от бруска металла отрубали нужный кусок, потом появились монеты.
Серебро в природе
Найти чистый металл можно нечасто. Большой его объем составляют сульфиты и глинистые сланцы. На тонну породы приходится 60–70 мг (максимум 1 г) драгоценного элемента.
Серебро выгодно добывать из золотосеребряных, медных и свинцовых руд. Есть разные соединения:
- Электрум — вид самородного золота, содержит до 50 % серебра. Соединение представлено пластинчатыми образованиями или дендритами белого, светло-желтого, зеленовато цвета. Бывает непрозрачным, с металлическим блеском.
- Аргентит — серебросодержащая руда, соединение с серой. Встречается сплошной массой, в пластинках или кристаллах. Бывает железно-черного или черновато-серого цвета. Соединение непрозрачно, имеет металлический блеск.
- Галенит — важнейший источник свинца. Кроме серебра может содержать кадмий, селен и другие примеси. Встречается сплошными массами и кубическими кристаллами. Характерен свинцово-серый цвет, непрозрачность и тусклый металлический блеск.
- Прустит — мышьяково-серебряная обманка. Встречается просвечивающими сплошными массами алого, багряно-красного, красновато-серого цвета. Характерен алмазный блеск и потемнение на свету.
- Пираргирит — сравнительно редкий минерал, является соединением с сурьмой, содержит почти 60 % серебра. Встречается дендритами, зернистыми вкраплениями, налетом. Бывает пурпурно-красного цвета, полупрозрачен, просвечивает. Характерен алмазный полуметаллический блеск.
- Стефанит (кислое, ломкое или черное серебро) — содержит почти 70 % драгоценного металла, а также серу и сурьму. Встречается сплошными массами и кристаллами серого или черного цвета.
Находят драгоценный металл также на месторождениях кварца, угля, нефти, полиметаллов. Морская вода содержит микроскопические частицы серебра, но добывать его при таких условиях трудно, поскольку необходимая технологическая база отсутствует. Для получения 1 г металла нужно 25 тысяч тонн морской воды.
Небольшое количество элемента содержат живые организмы. Драгоценный металл есть и в падающих на планету метеоритах.
Ученые подсчитали, что добыто было примерно 700 тысяч тонн серебра. Даже самородки распознать нелегко, так как металл покрывает темно-серый налет сульфида. Иногда он напоминает запутанную проволоку или сухой мох, имеет коричневатую или ржавую окраску. Такой эффект дает гидроксид железа, покрывающий металл.
ЗАПАСЫ И ДОБЫЧА
Серебро на акантите, 2.3 x 1.8 x 1.1 см, Перу, шахта Учукчакуа
По СССР крупные месторождения не известны. Самородки серебра в прежнее время находили в Турьинских рудниках на Северном Урале, в ряде свинцово-цинковых месторождений Алтая, Казахстана, Восточной Сибири и в других местах. Из иностранных месторождений большой известностью пользовались месторождения: Конгсберг(Норвегия), где самородное серебро встречалось до глубины 900 м, Кобальт(Канада), Шнееберг(Германия). Добыча серебросодержащих руд может производиться подземным или открытым способом. Сначала при помощи специальных приборов геологоразведчики проверяют шахты под землей на предмет содержания полезных ископаемых и драгоценных металлов. После обнаружения богатых серебром участков в соответствующих местах делают отверстия, в которые закладывают взрывчатку. Поднятые взрывом на поверхность шахты осколки серебросодержащей руды измельчают промышленным способом. Из руды драгоценный металл извлекают методами амальгации и цианирования.
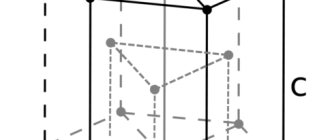
СТРУКТУРА
Кристаллическая структура серебра
Сингония кубическая; гексаоктаэдрический в. с. ЗL 4 4L6 3 6L 2 9РС. Кристаллическая структура. Гранецентрированный куб. Облик кристаллов. Правильно образованные кристаллы очень редки. Встречающиеся формы: , . Двойники по (111). Агрегаты. Встречается иногда в виде типичных «вязаных» перистых дендритов, тонких неправильных пластин и листочков. Характерны также моховидные, волосовидные и проводочные формы. Наиболее распространены зерна неправильной формы и более крупные сплошные скопления — самородки.
Как отличить от подделки
Серебро — благородный, драгоценный металл, который часто злоумышленники подделывают и продают под его видом в лучшем случае, металлы покрытие серебром или сплавы с низким содержанием аргентума. Чтобы выявить подделку, необходимо использовать свойства металла, в первую очередь теплопроводность. Привязать на нитку изделие и опустить в кипяток, через 0,5-1 мин. вытащить и ощупать, металл моментально становится горячим, в отличие от других.
Второй способ можно использовать и во время покупки серебра, острым предметом или иголкой (булавкой, острым ножом) провести по металлу (поцарапать) на нем не должно остаться следов.
Третий способ, по которому можно выявить драгоценный металл или цинк, нанести на изделие йод или лекарственный препарат с серой, если место потемнело, значит это подделка.
Серебро никогда не оставляет следов на коже, поэтому в ювелирном салоне перед покупкой, изделием нужно провести по коже, если на ней появятся темные полосы, то это подделка или сплав с низким содержанием аргентума.
Элементарным и самым простым способом можно назвать мел, им проводят по украшению. Мел, единственный материал, на котором остаются темные следы от серебра.
Во время покупки серебряных изделий, необходимо выбирать проверенные ювелирные салоны, а также учитывать стоимость серебра на рынке в текущий момент, что позволит выявить подделку.
Применение серебра
Уже с давних времен серебро использовали при изготовлении зеркал, в настоящее время его заменяют алюминием для удешевления производства. Низкое электрическое сопротивление серебра находит применение в электротехнике и электронике, тут из него изготавливают разнообразные контакты и разъемы. В настоящее время серебро практически не используют для производства монет, из него изготавливают только памятные монеты. Большая часть серебра используется в ювелирном деле, при изготовлении столовых приборов. Серебро также широко используется в химической и пищевой промышленности. Интересно применение иодида серебра. С его помощью можно управлять погодой. Распыляя ничтожные количества иодида серебра с самолета, добиваются образования водяных капель, т.е. проще говоря вызывается дождь. При необходимости можно выполнить и противоположную задачу, когда дождь совершенно не нужен, например, при проведении какого-то очень важного мероприятия. Для этого иодид серебра распыляют за десятки километров до места события, тогда дождь прольется там, а в нужном месте будет сухая погода. Серебро широко применяется в медицине. Его используют как зубные протезы, в производстве лекарств (колларгол, протаргол, ляпис и др.) и медицинских инструментов.
Серебряный столовый сервиз
Элементы таблицы Менделеева
Щелочные и щелочноземельные элементы
К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию. Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
| Щелочные металлы | Щелочноземельные металлы |
| Литий Li 3 | Бериллий Be 4 |
| Натрий Na 11 | Магний Mg 12 |
| Калий K 19 | Кальций Ca 20 |
| Рубидий Rb 37 | Стронций Sr 38 |
| Цезий Cs 55 | Барий Ba 56 |
| Франций Fr 87 | Радий Ra 88 |
Лантаниды (редкоземельные элементы) и актиниды
Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название «редкоземельные» элементы. Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
| Лантаниды | Актиниды |
| Лантан La 57 | Актиний Ac 89 |
| Церий Ce 58 | Торий Th 90 |
| Празеодимий Pr 59 | Протактиний Pa 91 |
| Неодимий Nd 60 | Уран U 92 |
| Прометий Pm 61 | Нептуний Np 93 |
| Самарий Sm 62 | Плутоний Pu 94 |
| Европий Eu 63 | Америций Am 95 |
| Гадолиний Gd 64 | Кюрий Cm 96 |
| Тербий Tb 65 | Берклий Bk 97 |
| Диспрозий Dy 66 | Калифорний Cf 98 |
| Гольмий Ho 67 | Эйнштейний Es 99 |
| Эрбий Er 68 | Фермий Fm 100 |
| Тулий Tm 69 | Менделевий Md 101 |
| Иттербий Yb 70 | Нобелий No 102 |
Химические соединения
Для образования такого соединения, как хромат серебра, необходима хромовая кислота и сам благородный металл. Реакция не является часто встречающейся в природе и гораздо чаще происходит в лабораторных условиях. Если в лаборатории хранится серебро, формула этого вещества сразу записывается на электронный носитель информации.
Хромат серебра имеет вид красноватых кристаллов ромбической формы. Они почти не растворяются в воде и имеют парамагнетические свойства.
При взаимодействии с фтором образуется фторид серебра. Данное вещество считается бинарным соединением неорганического происхождения. Нужно отметить, что данное вещество практически не используется в промышленности. Фторид серебра выглядит как порошок буровато-зеленого цвета. Он тоже может иметь кристаллическую форму. Данное различие обусловлено разницей в агрегатных состояниях первоначальных составляющих. В таких случаях даже может выделиться сульфат серебра.
Украшения и бытовое использование
Для изготовления украшений или иных изделий используют слитки содержанием серебра от 99,9% до 99,99%. Самыми дорогостоящими считаются изделия с 925 пробой.
Металл нашел широкое применение в большинстве отраслей промышленности:
- машиностроении;
- приборостроении;
- изготовление фото и видео аппаратуры;
- электронике;
- электротехнике;
- чеканке монет;
- медицине.
Металл обладает высокой электропроводностью и теплопроводностью, что является очень важным свойством при производстве деталей.
Для создания ювелирных украшений применяют самородное серебро с примесями меди, никеля. Известные бренды обрабатывают серебряные предметы белым родием, чтобы они не теряли своего первозданного блеска и вида.
Брендов по изготовлению изделий из серебра большое количество, каждый имеет свою специализацию, одни делают часы, другие кольца, серьги, третье выполняют фигуры и статуэтки. Среди них:
- AGNI;
- Damiani;
- Boucheron;
- Akvamarin;
- Argentina Bortolotti;
- Balmain;
- Tiffany and Co;
- Gava.Cool;
- Cote and Jeunot by Lena Yastreb;
- Cartier SA;
- Bvlgari (Bulgari);
- Baraca;
- Gucci.
Очищение металла
- Руда помещается в резервуар, обрабатывается цинковой пылью. В результате все примеси оседают на дно, целевое сырье остается наверху. Последующая очистка производится на заводах.
- Пирометаллургический метод позволяет получить чистое серебро. В качестве концентраторов нужно использовать медь или свинец. Эти вещества обрабатываются цинком под воздействием температуры 450 градусов – так частички металла лучше растворяются. После извлечения застывшей субстанции от нее отделяют драгметалл.
- При температуре 1250 градусов цинк испаряется, но в оставшемся серебре все еще содержится мышьяк и свинец. Для очистки используется обработка кислородом и тепловое воздействие 1000 градусов. Этот способ наиболее выгодный, поскольку свинец и медь добываются в больших количествах. Переработка таких элементов не требует значительных затрат.
- Очищенный драгметалл переплавляется в слитки. Ни одна технология не дает гарантии получения на 100% чистого серебра. Чтобы полностью избавиться от примесей, слитки переправляют на металлургические предприятия для последующей обработки.
Если в качестве основного сырья используется медь или свинец, применяется пирометаллургическая методика очистки. Такой способ отличается выгодой, поскольку эти примеси недорогие. В итоге цена процесса производства уменьшается, окупаются затраты на изготовление менее дорогостоящих металлов. Для отделения серебра используется технология электрохимической очистки.
Фототехника и электроника
Использование нитрата и галогенида серебра для изготовления фотографий в последнее время теряет актуальность, ведь с появлением цифровых технологий спрос на цветную пленку начал стремительно падать. Пик мирового спроса на фотографическое серебро приходился на 1999 год. Теперь же устаревшая пленочная фототехника постепенно исчезает даже в странах третьего мира.
В электротоварах этот металл используется для превосходной проводимости тока. Некоторые производители электротехники выпускают соединительные, силовые кабели и провода акустических систем, используя серебряные проводники высшего качества.
Их проводимость на 6% выше, чем у идентичных медных аналогов, но и стоят они заметно дороже. Как ни странно, спрос на подобную продукцию довольно большой. Многие меломаны-энтузиасты уверяют, что такие проводники в аудиосистемах улучшают качество звука, но научно это не было доказано.
Небольшие устройства, такие как часы и слуховые аппараты, обычно используют серебряные батареи. Причина состоит в том, что масса данного металла относительно небольшая, а энергосберегающие свойства очень хорошие. Он также применяется для изготовления серебряно-цинковых и серебряно-кадмиевых аккумуляторов. Кроме того, оксид серебра кадмий используется в высоковольтных контактах.
Сочетания с камнями и другими металлами
Ювелиры сочетают серебро со многими дорогими и дешевыми металлами, чаще при производстве украшений соединяют с ним золото, платину. Также нет исключений в оправе серебром драгоценных, полудрагоценных или поделочных камней. Мировые бренды в серебро оправляют рубины, жемчуг, изумруды, бриллианты, менее известные заводы и фирмы — фианиты, гранат, янтарь и другие камни.
Достоинства и недостатки
Преимущества:
- Серебряные украшения подходят под любую одежду. Этого нельзя сказать о золоте. Золотые изделия могут испортить внешний вид человека. Оно часто затмевает вид одежды, привлекая повышенное внимание.
- Золотые украшения принято надевать на большие празднования, церемонии. Серебро же подойдет на любой праздник, деловую встречу, собеседование.
- Серебряные украшения подходят и мужчинам, и женщинам. Преобладающих факторов по гендерному различию нет.
- Долговечность, прочность, износоустойчивость.
Серьезных недостатков у этого металла нет за исключением того, что со временем он темнеет.
Влияние серебра на человека
Как мы видели выше, использование небольших доз серебра имеет обеззараживающее и бактерицидное действие. Однако, что полезно в малых дозах, очень часто бывает губительно в больших. Серебро здесь не исключение. Повышение концентрации серебра в организме может вызвать снижение иммунитета, повреждения почек и печени, щитовидной железы и головного мозга. В медицине описаны случаи нарушения психики при отравлении серебром. Многолетнее поступление серебра в организм малыми дозами приводит к развитию аргирии. Металл постепенно откладывается в тканях органов и придает им зеленоватый или голубоватый цвет, особенно виден этот эффект на коже. При тяжелых случаях аргирии кожа темнеет настолько, что становится похожа на кожу африканцев. Кроме косметического эффекта в остальном аргирия не оказывает какого то ухудшения самочувствия и расстройства работы организма. Но и тут имеется свой плюс, при том, что организм пропитан серебром, ему становятся нипочем любые инфекционные заболевания!
Американец Пол Карсон «Папа Смурф», страдавший аргирией